揭開轉錄因子的非轉錄功能:成大團隊揭開 miRNA 調控新視角
(中央社訊息服務20241126 10:33:56)今年的諾貝爾生理醫學獎頒給了發現微型核糖核酸(microRNA,簡稱 miRNA)的團隊,可見其重要性,國立成功大學醫學院醫學檢驗生物技術學系陳百昇老師團隊經過多年努力,發現缺氧誘發因子(HIF-1α)在非轉錄層面上可動態調控 miRNA 成熟化的新機制,解開更上游的未知謎團,研究成果已刊登在英國牛津大學出版的國際頂尖期刊「核酸研究(Nucleic Acids Research)」上,受到國際矚目。

陳百昇指出,這項傑出的研究成果,主要歸功於第一作者李婕寧博士後研究員多年奮鬥,團隊中還包括醫技系阮振維老師、助理呂瑜珍、博士生翁沂秀等人,都是成大校內包括基礎醫學研究所、醫技系與微生物及免疫學研究所自行訓練出來的人才,相當不容易。
李婕寧表示,在分子生物學研究中,因為很多東西太微小,看不到摸不到,需要許多想像與摸索,才能獲得證實,這項研究前後歷經8年,過程中經歷無數次失敗的「撞牆期」,如果不是因為熱愛可能早就放棄,也因團隊成員彼此鼓勵才能堅持下去。
陳百昇表示,大家熟知的分子生物學「中心法則」亦即遺傳訊息經由去氧核醣核酸(DNA)轉錄為編碼型核醣核酸(coding mRNA),再轉譯為蛋白質以執行各項功能之過程。一直以來,核醣核酸(RNA)僅被當作中間傳遞訊息之產物,導致於忽略其功能。有趣的是,科學家後來發現,短鏈的 miRNA 雖然短小,且不轉譯出蛋白質,卻可藉由結合 coding mRNA 來調控遺傳訊息之表現量,成為特定基因最終是否能成功轉譯的重要關鍵。說明了 RNA 不僅僅只有傳遞訊息之中間角色,還具有直接的基因調控能力。
李婕寧表示,在惡性腫瘤的發展過程中,HIF-1α 是一個重要且經典的轉錄因子,透過在細胞核內直接調控代謝、血管新生等等和腫瘤惡化相關基因的表達,維持癌細胞在缺氧環境中的存活優勢。過去的研究也觀察到癌症患者 miRNA 生合成異常,原因卻不清楚。
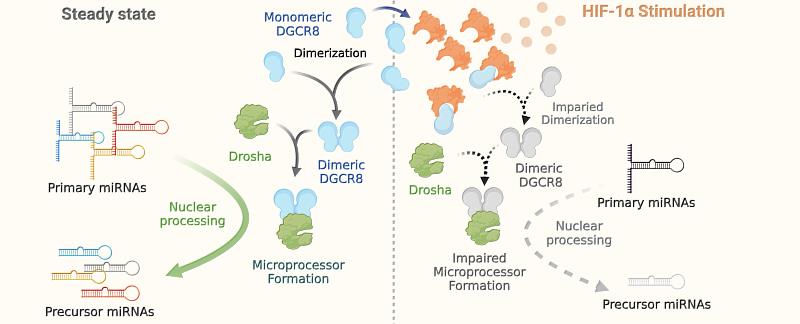
在研究團隊的多年努力之下,成功揭示了 HIF-1α 在非轉錄層面上動態調控 miRNA 成熟化的新機制。在分子層面上,HIF-1α 透過蛋白質結合、「綁架」了 DGCR8(miRNA 生合成蛋白質)單體,進而抑制 DGCR8 雙體形成、阻礙細胞核內的 Drosha-DGCR8 微處理器的組裝,影響 miRNA 的核內成熟。也就是 HIF-1α 除了轉錄因子之功能外(結合 DNA),竟然還可以透過綁架特定蛋白質,抑制 miRNA 的初始生成。
李婕寧表示,此一嶄新機制除了在惡性腫瘤微環境會受到缺氧條件或是生長因子刺激而啟動,也在人類各種細胞中,甚至是其他生物模式如線蟲和果蠅中可觀察到相似的現象,顯示這是廣泛存在的生物調控機制。此研究成果,不僅補足 miRNA 生合成異常在癌症中的關鍵拼圖,更是未來發展基於 miRNA 調控創新療法的重要基礎。

陳百昇表示,2006 年諾貝爾生理醫學獎,Andrew Fire 和 Craig Mello 因發現 RNA 干擾(RNA interference, RNAi)及其在基因沉默(生物細胞藉由各種基因表現調控機制抑制某一基因表現的現象)中的關鍵作用獲得該獎項。
而在 2024 年的諾貝爾生理醫學獎,Victor Ambros 和 Gary Ruvkun 因發現 miRNA 在基因調控中的核心作用而獲獎,他們的研究顯示 miRNA 對多細胞生物的發育和功能至關重要。
陳百昇指出,歷年諾貝爾生醫獎中,與 RNA 相關至少有 5 次,2019 年更頒給發現 HIF-1α 在缺氧相關的研究團隊,而成大團隊這次獲得刊登的期刊,在生醫領域排名前 2%,顯示團隊以有限的資源,仍能擠身全球之列,一較長短。研究團隊除了特別感謝國家科學及技術委員會獎項計劃的補助,成大校內各項完善設施的支援也功不可沒,也尤其感謝實驗室成員們不懈的努力與堅持。





